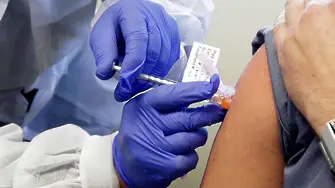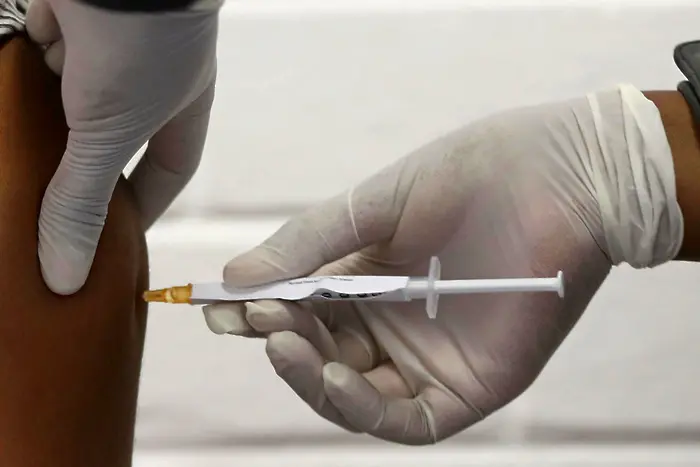
Американският фармацевтичен гигант Pfizer и германската BioNTech са подали молба за спешно одобрение на своята ваксина за коронавируса, чиито ранни резултати бяха представени преди седмица и показваха 95% ефикасност.
Те са подали документи към съответните здравни регулатори в САЩ, Австралия, Канада, Европа, Япония, Великобритания. Надяват се бързо одобрение да позволи първи дози от ваксината да стигнат до високорискови хора до края на декември.
Много здравни регулатори имат подобни програми, които позволяват бързо одобрение на лекарства, ако данните от ранните тестове са покрили достатъчно изисквания. Засега ваксината на Pfizer/BioNTech e тествана върху над 40 000 души.
В САЩ ще бъдат предоставени данните от 170 участници в тестовете, част от които са се заразили въпреки ваксината (останалите са били на плацебо), данни за безопасността, получени от 8000 души, както и допълнителни данни за 38 000 от участниците.
Ваксината е базирана на нова технология - mRNA - която на практика дава на тялото ни инструкции как да създаде антитела и Т-клетки срещу SARS-CoV-2 - вирусът, който причинява COVID-19. Тази технология досега не е ползвана за успешен медицински продукт или ваксина, но дава добри резултати и предизвиква силен имунен отговор сред тестваните.
Ваксината на Pfizer/BioNTech е една от първите ваксини срещу COVID-19, която ще види бял свят. Очакват се скоро подобни молби и от Moderna, AstraZeneca/Оксфорд и други.
Подкрепете ни
Уважаеми читатели, вие сте тук и днес, за да научите новините от България и света, и да прочетете актуални анализи и коментари от „Клуб Z“. Ние се обръщаме към вас с молба – имаме нужда от вашата подкрепа, за да продължим. Вече години вие, читателите ни в 97 държави на всички континенти по света, отваряте всеки ден страницата ни в интернет в търсене на истинска, независима и качествена журналистика. Вие можете да допринесете за нашия стремеж към истината, неприкривана от финансови зависимости. Можете да помогнете единственият поръчител на съдържание да сте вие – читателите.
Подкрепете ни